功能主治:用于重症肌无力、脊髓灰质炎后遗症、由于神经系统的疾病或外伤所引起的感觉及运动障碍、多发性神经炎及脊神经炎及拮抗氯化筒箭毒碱及类似药物的非去极化肌松作用。
查看说明书药品对比
| 药品信息 | |||
| 主要成分 |
本品主要成分为氢溴酸加兰他敏。化学名称:(4αS,6R,8αS)-11-甲基-3-甲氧基-4α,5,9,10,11,12-六氢-6H-苯并呋喃并[3α,3,2-ef][2]苯并氮砸卓-6-醇氢溴酸盐分子式:C17H21NO3.HBr分子量:368.27辅料:氯化钠、注射用水。 |
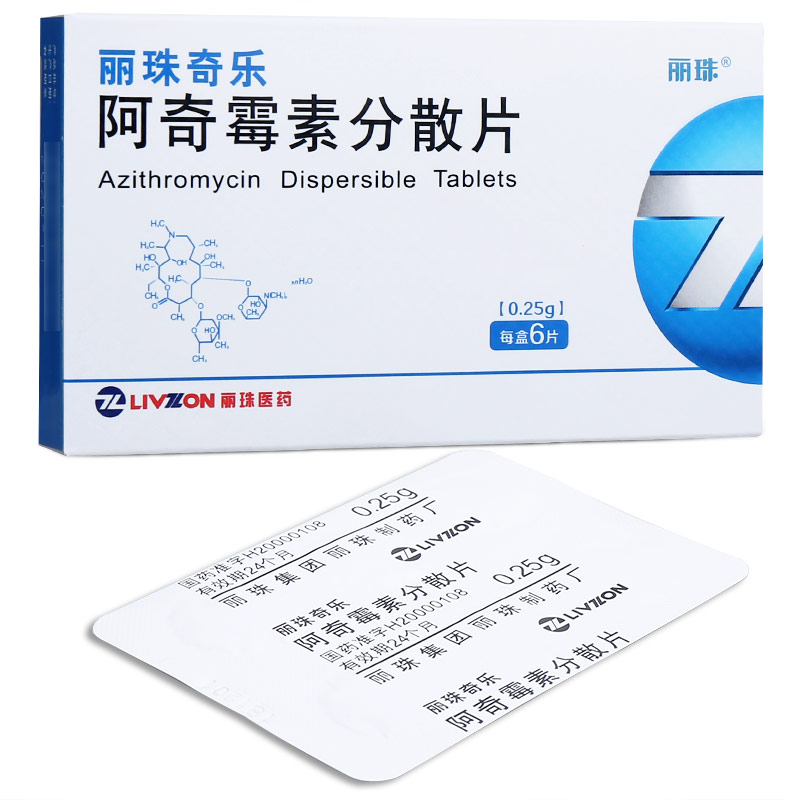
阿奇霉素。 |
|
| 生产企业 |
遂成药业股份有限公司 |
丽珠集团丽珠制药厂 |
|
| 批准文号 |
国药准字H41023666 |
国药准字H20000108 |
|
| 说明 | |||
| 作用与功效 |
用于重症肌无力、脊髓灰质炎后遗症、由于神经系统的疾病或外伤所引起的感觉及运动障碍、多发性神经炎及脊神经炎及拮抗氯化筒箭毒碱及类似药物的非去极化肌松作用。 |
本品适用于敏感细菌所引起的下列感染:中耳炎、鼻窦炎、咽炎、扁桃体炎等上呼吸道感染:支气管炎、肺炎等下呼吸道感染。皮肤和软组织感染。沙眼衣原体所致单纯性生殖器感染。非多重耐药淋球菌所致的单纯性生殖器感染(需排除梅毒螺旋体的合并感染)。 |
|
| 用法用量 |
肌内或皮下注射一次2.5~10mg(0.5~2支),一日1次,必要时一昼夜可注射2次,极量一日20mg(4支)。小儿按体重一次0.05~0.1mg/kg。 抗箭毒:肌内注射起始剂量5~10mg(1~2支),5或10分钟后按需要可逐渐增加至10~20mg(2~4支)。 |
以阿奇霉素分散片治疗感染性疾病,其疗程及使用方法如下:用水分散后口服或直接吞服成沙眼衣原体或敏感淋球菌所致性传播疾病,仅需单次口服本品1.0g.对其他感染的治疗:总剂量1.5g,分三次服药;一日1次服用本品0.5g。或总剂量相同,仍为1.5g,首日服用0.5g,然后第二至第五日一日1次口服本品0.25g.如发生超量使用(尚未有报道),可进行洗胃或用一般支持疗法。 |
|
| 副作用 |
癫痫、运动机能亢进、机械性肠梗阻、支气管哮喘、心绞痛和心动过缓者均忌用。青光眼患者不宜使用。 |
(一)临床试验经验:由于临床试验在不同的条件下完成,在临床试验中观察到的一种药物的不良反应率不能直接和其他药物在临床试验中的不良反应率相比较,且未必反映在实际应用中的不良反应率。阿奇霉素静脉制剂治疗社区获得性肺炎的临床试验中,静脉给药2~5个剂量,所报道的不良反应多数为轻至中度,且停药后可恢复。这些临床试验中多数患者有一种以上合并症,并需应用其他药物。约1.2%用本品静脉制剂的患者中止用药,2.4%采用静脉或口服阿奇霉素治疗的患者因出现不良反应症状或实验室检查异常而中止用药。在盆腔炎性疾病患者中进行的临床试验中,接受阿奇霉素单药治疗的女性患者静脉给药1~2个剂量后,2%患者因临床不良反应而停药,阿奇霉素与甲硝唑合用的患者中4%的患者因不良反应而中止治疗。以上研究中,导致停药最常见的不良反应为胃肠道反应(腹痛、恶心、呕吐、腹泻等)和皮疹,导致停药的实验室检查异常主要为氨基转氨酶和/或碱性磷酸酶升高。在社区获得性肺炎的研究中,成年患者接受本品静脉/口服制剂治疗后最常见的不良反应为胃肠道反应,其中腹泻或稀便(4.3%),恶心(3.9%),腹痛(2.7%),呕吐(1.4%)。约12%的患者发生 |
|
| 禁忌 |
|
孕妇及哺乳期妇女用药:动物生殖毒性研究表明阿奇霉素穿过胎盘,但对胎儿无损害迹象,尚无本品在母乳中的分泌资料。在人的妊娠,哺乳期使用的安全性迄今尚未证实,故在妊娠或哺乳期妇女无适当选择余地时才使用本品。儿童用药:尚不明确。老年用药:可参见【注意事项】项。 |
|
| 成分 |
用于重症肌无力、脊髓灰质炎后遗症、由于神经系统的疾病或外伤所引起的感觉及运动障碍、多发性神经炎及脊神经炎及拮抗氯化筒箭毒碱及类似药物的非去极化肌松作用。 |
本品适用于敏感细菌所引起的下列感染:中耳炎、鼻窦炎、咽炎、扁桃体炎等上呼吸道感染:支气管炎、肺炎等下呼吸道感染。皮肤和软组织感染。沙眼衣原体所致单纯性生殖器感染。非多重耐药淋球菌所致的单纯性生殖器感染(需排除梅毒螺旋体的合并感染)。 |
|
| 药理作用 |
治疗剂量偶致过敏反应。 |
||
| 注意事项 |
未进行该项试验且无可靠参考文献。 |
1. 服用期间避免饮酒;2. 孕妇及哺乳期妇女慎用;3. 肝肾功能不全患者应在医生指导下使用;4. 过敏体质者慎用;5. 按医嘱剂量服用,不宜自行增减剂量。 |
|